Dilatação dos Líquidos
A dilatação de um sólido com o aumento de temperatura ocorre porque com o aumento da energia térmica aumentam as vibrações dos átomos e moléculas que formam o corpo, fazendo com que passem para posições de equilíbrio mais afastadas que as originais.
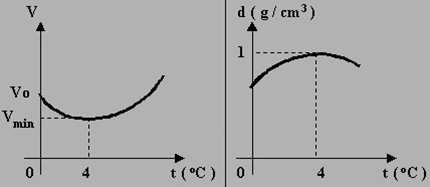
OBS.: Na água ocorre fenômeno inverso de 0 a 4ºC. Portanto para dada massa de água, a 4ºC ela apresenta um volume mínimo. Lembrando que a densidade é dada pela relação entre a massa e seu volume (d = m/v), concluímos que a 4ºC a água apresenta densidade máxima.

Esse comportamento da água explicam por que, nas regiões de clima muito frio, os lagos chegam a ter suas superfícies congeladas, enquanto no fundo a água permanece líquida a 4ºC. Como a 4ºC água tem densidade máxima, ela permanece no fundo não havendo possibilidade de se estabelecer o equilíbrio térmico por diferença de densidade.
No estado sólido, os átomos de oxigênio, que são muito eletronegativos, unem-se aos átomos de hidrogênio através da ligação denominada ponte de hidrogênio. Em consequência disso, entre as moléculas, formam-se grandes vazios, aumentando o volume externo (aspecto macroscópico). Quando a água é aquecida de 0°C a 4°C, as pontes de hidrogênio rompem-se e as moléculas passam a ocupar os vazios existentes, provocando, assim, uma contração.
Portanto, no intervalo de 0°C a 4°C, ocorre, uma diminuição de volume. Mas, de 4°C a 100°C, a água dilata-se de modo normal. Então, a 4°C, tem-se o menor volume para a água e, assim a maior densidade da água no estado líquido.
OBS: A densidade da água no estado sólido (gelo) é menor que a densidade da água no estado líquido.
Primeiras noções – Escalas Termométricas
O termo tem sua origem na sensação de “Quente” ou “Frio”, que podemos sentir pelo contato com o corpo.
Através do sentido do tato podemos constatar que as propriedades do corpo variam, quando ele se aquece ou se resfria. Vejam os exemplos a seguir:
- Uma barra, um fio, alonga‑se quando o aquecemos; é o fenômeno da Dilatação Linear.
- Um sólido aumenta o volume quando aquecido; é o fenômeno da Dilatação Cúbica.
- Ao aquecer um balão de vidro cheio d’água, o nível baixa a princípio, devido à dilatação do invólucro, mas sobe depois além do nível primitivo, o que mostra que a dilatação dos Líquidos é, em geral maior do que a dos sólidos.
- Quando se mantém constante a pressão, um gás aumenta o seu volume com o aquecimento.
- A resistência elétrica de um fio metálico aumenta quando o aquecemos. Seja um fio condutor levado ao vermelho sombrio pela corrente elétrica que o percorre e resfriado por imersão em água de urna parte do fio. A parte não mergulhada se torna vermelho vivo, o que indica passagem de corrente mais intensa e, portanto, diminuição da resistência na parte mergulhada.
Em resumo, sem tocá‑lo, podemos saber se um corpo se aquece ou se resfria mediante o exame da variação de uma de suas propriedades.
Temperatura
Todas as substâncias são constituídas de pequenas partículas, as moléculas, que estão em contínuo movimento.
Quanto mais rápido o movimento das moléculas mais quente o corpo e quanto mais lento mais frio.
Calor
“O Calor consiste no movimento das partículas de um corpo” – Isaac Newton
É a energia cinética das moléculas, energia em trânsito.

Equilíbrio Térmico
Do maior potencial ao menor. Ausência de troca de energia entre os corpos.
Quanto maior a temperatura de um corpo, maior a vibração das moléculas.
Estrutura do Sólido
Nos sólidos, as moléculas vibram em torno de posições fixas.
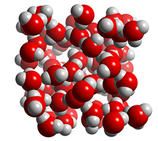
Estrutura do Líquido
Nos líquidos as moléculas vibram, mas mudam constantemente de posições.
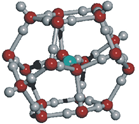
Estrutura do gás
No gás, as moléculas movem-se livremente a grande velocidade e sem nenhuma ordem.
MODOS DE TRANSMISSÃO DE CALOR
A TRANSMISSÃO DE CALOR É DEFINIDA COMO A ENERGIA DE UMA REGIÃO A OUTRA, SENDO A DIFERENÇA DE POTENCIAL TÉRMICO ENTRE ELAS.
Se um bloco quente de cobre é colocado num recipiente com água fria, observa‑se que o cobre esfria e a água se aquece, até que seja atingido o equilíbrio de temperatura.
Os aumentos da temperatura da água e queda da temperatura do cobre são devidos a passagem de uma forma de energia do cobre para a água. Dessa energia chega‑se ao conceito de calor.
“O CALOR é definido como sendo a forma de energia que é transferida através da fronteira de um sistema, em virtude da diferença de temperatura”.
A transmissão de calor pode ser definida como a transmissão de energia de uma região a outra, como resultado da diferença de temperatura entre elas.
Como existem diferenças de temperaturas em todo o universo, os fenômenos de fluxo de calor são tão universais quanto os associados às atrações gravitacionais.
Ao contrário da gravidade, entretanto, o fluxo de calor não é governado por uma única relação, mas por uma combinação de várias leis da física.
Temos três modos distintos de transmissão de calor: CONDUÇÃO, RADIAÇÃO e CONVECÇÃO.
CONDUÇÃO
A condução é um processo pelo qual o calor flui de uma região de alta temperatura para outra mais baixa, dentro de um meio (sólido, líquido ou gasoso) ou entre meios diferentes em contato físico direto.
No fluxo de calor por condução a energia é transmitida por meio de comunicação molecular direta, sem apreciável deslocamento das moléculas.
RADIAÇÃO
A radiação ou calor radiante é um processo pelo qual o calor flui de um corpo de alta temperatura para um de baixa quando eles estão separados no espaço, ainda que exista um vácuo entre eles.
O CALOR RADIANTE, NO VÁCUO, ATINGE A VELOCIDADE DA LUZ DE 300 mil km/s.
O termo radiação é em geral aplicado para todas as espécies de fenômenos de ondas eletromagnéticas. Na transmissão de calor, são de interesse apenas os fenômenos que resultam da diferença de temperatura e podem transportar energia através de um meio onde exista o vácuo ou através do espaço.
Essa energia é o Calor Radiante.
Todos os corpos emitem calor radiante de modo constante. A intensidade das emissões depende da temperatura e da natureza da superfície.
A energia radiante tem a velocidade da luz (300 mil km/s) como à radiação da luz.
De fato, de acordo com a teoria eletromagnética, a luz e a radiação térmica diferem apenas nos comprimentos de onda.
O calor radiante irradia de um corpo na forma de impulsos ou “quantum” de energia.
CONVECÇÃO
A convecção é um processo de transporte de energia pela ação combinada da condução de calor, armazenamento de energia e movimento de mistura. A convecção é mais importante como mecanismo de transferência de energia (calor) entre uma superfície sólida e um líquido ou gás.

DILATAÇÃO TÉRMICA DOS CORPOS
De um modo geral, quando aumenta a temperatura de um corpo (sólido ou líquido), aumenta também a agitação das partículas que formam esse corpo.
Isso causa um afastamento entre as partículas, e assim um aumento nas dimensões do corpo (dilatação térmica).
Por outro lado, uma diminuição na temperatura de um corpo acarreta uma redução em suas dimensões.
Na construção civil, por exemplo, para prevenir possíveis trincas e rupturas por causa da dilatação térmica dos materiais, utilizam-se as ” folgas”, chamados de juntos de dilatação.
De maneira geral, os líquidos dilatam-se sempre mais que os sólidos ao serem igualmente aquecidos.
Dilatação Linear
Embora a dilatação de um sólido ocorra em todas as dimensões, pode predominar a dilatação de apenas uma das suas dimensões sobre as demais.
Ou, ainda, podemos estar interessados em uma única dimensão do sólido.
Dilatação Superficial
É a variação da área de uma placa quando submetida a uma variação de temperatura.
Dilatação Volumétrica
Vamos considerar a variação de volume, isto é, a dilatação nas três dimensões do sólido (comprimento, largura e altura).
DILATAÇÃO DA ÁGUA
A dilatação de um sólido com o aumento de temperatura ocorre porque com o aumento da energia térmica aumentam as vibrações dos átomos e moléculas que formam o corpo, fazendo com que passem para posições de equilíbrio mais afastadas que as originais.
OBS.: Na água ocorre fenômeno inverso de 0 a 4ºC. Portanto para dada massa de água, a 4ºC ela apresenta um volume mínimo. Lembrando que a densidade é dada pela relação entre a massa e seu volume (d = m/v), concluímos que a 4ºC a água apresenta densidade máxima.
O comportamento da água explicam por que, nas regiões de clima muito frio, os lagos chegam a ter suas superfícies congeladas, enquanto no fundo a água permanece líquida a 4ºC. Como a 4ºC água tem densidade máxima, ela permanece no fundo não havendo possibilidade de se estabelecer o equilíbrio térmico por diferença de densidade.
DILATAÇÃO DE CORPOS “OCOS”
“Corpos ocos se dilatam como se não fossem ocos.”
Exemplos:
a) Um anel de aço, ao se dilatar, comporta-se como um disco de aço.
b) Um furo em uma chapa de ferro se dilata, quando aquecido, como se fosse feito de ferro .
c) Um cubo oco de cobre se dilata, quando aquecido, como se fosse sólido.
A importância da teoria e dos conceitos – Dilatação dos Líquidos
Conceitos, definições, norma ou boas práticas de engenharia que são importantes para que possamos ter o perfeito entendimento e aplicar na prática.
Em conclusão, você conhece o Canal no YouTube? Portanto assista aos melhores vídeos de sensores de temperatura de contato e sem contato da internet.
A teoria e os conceitos em Termopar – Dilatação dos Líquidos
Conceitos, definições, norma ou boas práticas de engenharia que são importantes para que possamos ter o perfeito entendimento e aplicar na prática.
Em conclusão, você conhece o Canal no YouTube? Portanto assista aos melhores vídeos de sensores de temperatura de contato e sem contato da internet.
Como resultado dos vídeos do Canal no YouTube os profissionais de manutenção elétrica e instrumentação terão uma evolução significativa de seus conhecimentos.
Site Termopares desde 1999 e Dilatação dos Líquidos
O site Portal Termopares está no ar desde 1999 e, portanto, o mais confiável e imparcial onde se encontra o melhor conteúdo da internet em medição industrial de temperatura.
Hoje o Canal no YouTube tem mais de 300 vídeos sobre termometria Industrial e assim se destaca como uma das principais fontes de informação da internet.
Para esclarecer o portal termopares é um lugar onde encontramos toda teoria sobre sensores de temperatura e de um modo imparcial pois não nos preocupamos com a questão e sim a questão técnica.
Portal Termopares desde 1999 o mais antigo e certamente o mais confiável da internet.
Sem dúvida a grandeza temperatura é uma das mais importantes medidas controladas na indústrias.
Dilatação dos Líquidos você encontra no Livro Nível Básico

Visite a Loja virtual do Curso Termometria. Acima de tudo adquira hoje mesmo a sua apostila nível básico especialmente desenvolvida para estudantes e usuários da indústria.
Visite a loja e compre hoje mesmo!!
Em resumo, uma loja virtual confiável onde poderá adquirir a apostila e ainda dividir no cartão de crédito.
Um curso de termometria nível básico em forma de apostila onde é tratado os conceitos da termometria, mas também uma forma de preparar seus estudos para a apostilas de nível intermediário e avançado. Acima de tudo uma obra que não pode faltar para o seu desenvolvimento profissional.

WhatsApp: +55 11 97771-7772
Livro Nível Intermediário, tem Dilatação dos Líquidos

Nível Intermediário destinado ao uso e a aplicação de Termopar e Pt100
Sem dúvida o mais importante conteúdo de termometria e ainda exclusivo.
Conteúdo exclusivo e acima de tudo baseado em uma experiência profissional de mais de 35 anos!
Visite a loja e compre hoje mesmo!!
O pagamento é facilitado no cartão de crédito!! O mais importante é ser um inscrito no canal curso termometria (YouTube) e assim poderá solicitar o seu cupom de desconto.
Um verdadeira obra onde o objetivo é deixar um legado de mais de 35 anos anos de experiência em medição de temperatura industrial.
WhatsApp: +55 11 97771-7772
Livro Nível Avançado tem normas que trata da Dilatação dos Líquidos

Sem dúvida o melhor conteúdo conteúdo totalmente exclusivo e didático
Uma obra exclusiva, onde temos os melhores pontos em normas, teorias e boas práticas de engenharia para dimensionamento, mas também focada em aplicações em sensores.
Ideal para instalação de sensores em tubulações, mas também aplicações em tanques, fornos, estufas, mancais entre outros.
Conteúdo exclusivo e acima de tudo baseado em uma experiência profissional de mais de 35 anos!!
O pagamento é facilitado no cartão de crédito!! Mas se for um inscrito no canal curso termometria (YouTube) peça hoje mesmo seu cupom de desconto.
Um verdadeira obra onde o objetivo é deixar um legado de mais de 35 anos anos de experiência em medição de temperatura industrial.
WhatsApp: +55 11 97771-7772
Pontos importantes do Portal Termopares – Dilatação dos Líquidos
Em conclusão o Portal Termopares é a melhor fonte de conhecimento em sensores de temperatura da Internet.
Como resultado dos vídeos do Canal no YouTube os profissionais de manutenção elétrica terão com certeza uma evolução técnica.
O site Portal Termopares está no ar desde 1999 e, portanto, o mais confiável e imparcial onde se encontra o melhor conteúdo da internet em medição industrial de temperatura.
Diferenciais do Curso Termometria – Dilatação dos Líquidos
Hoje o Canal no YouTube tem mais de 300 vídeos em solução industrial em temperatura e assim se destaca como uma das principais fontes de informação da internet.
Para esclarecer o portal termopares é um lugar onde encontramos toda teoria sobre sensores. Atuamos de um modo imparcial pois não atuamos com a questão comercial e sim a questão técnica.
Termopares são fios metálicos de materiais diferentes que quando soldados e aquecidos neste ponto, observa-se uma carga em milivolts que se apresenta de modo proporcional a temperatura, e assim são elementos que se assemelham a termo pilhas.
Pontos destaque do Portal Dilatação dos Líquidos
Por exemplo, uma questão muito importante: Quais os motivos para consultar sobre sensores no Portal Termopares?
Ele é importante pelo fato de não ser um portal comercial já é um diferencial onde apresenta soluções totalmente imparciais, mas também porque valoriza o benefício ao cliente como sendo o ponto mais importante.
Você precisa por exemplo saber sobre instalar e projeto de sensores de temperatura, o melhor lugar é o Portal Termopares.
Precisa por exemplo de material didático para poder ler e consultar sempre que necessário o melhor lugar para encontrá-los é em nossa loja virtual.
Se precisar por exemplo de curso on-line.
Portal Termopares desde 1999 o mais antigo e certamente o mais confiável da internet.
Use seu cartão de crédito!! Se for inscrito no Canal no YouTube e peça hoje mesmo seu cupom de desconto.
Sem dúvida a grandeza temperatura é uma das mais importantes medidas controladas na indústrias.
O mais importante é ser um inscrito no Canal no YouTube e assim poderá solicitar o seu cupom de desconto.
Canal Curso no YouTube – Dilatação dos Líquidos
Como resultado dos vídeos do Canal no YouTube é para os profissionais de manutenção elétrica terão uma evolução cultural significativa.
O site Portal Termopares está no ar desde 1999 e, portanto, o mais confiável e imparcial onde se encontra o melhor conteúdo da internet em medição industrial de temperatura.
Hoje o Canal no YouTube tem mais de 300 vídeos sobre solução em temperatura industrial e assim se destaca como uma das principais fontes de informação da internet.
Para esclarecer o portal termopares é um lugar onde temos toda teoria sobre sensores e de um modo imparcial pois não se envolve a questão comercial e sim a questão técnica.
Portal Termopar e Pt100 uma fonte de consulta e tem Dilatação dos Líquidos
Você precisa por exemplo saber sobre como instalar sensores, o melhor lugar é o Portal Termopares.
Precisa por exemplo de material didático para poder ler e consultar sempre que necessário o melhor lugar para encontrá-los, visite nossa loja virtual.
Se precisar por exemplo de curso on-line entre aqui.
O Livro nível avançado, uma obra onde temos os melhores pontos em normas, teorias e boas práticas de engenharia.
Importante ao dimensionar sensores e também focado em aplicações em sensores.
O Livro nível avançado é ideal para instalação de sensores em tubulações, mas também aplicações em tanques, fornos, estufas, mancais entre outros.





